来源:智药局 最近,来自华盛顿大学David Baker教授课题组联合哈佛大学的科学家,描述了两种深度学习方法来设计指定的功能位点的蛋白质,而无需指定的的蛋白质二级结构。
7月22日,论文以“Scaffolding protein functional sites using deep learning”为题发表在Science杂志上。
01、文章概述
蛋白质的生化功能通常由构成功能位点的残基子集执行,因此具有新功能的蛋白质的设计可分为两个步骤。
第一步:确定功能位点的空间结构和氨基酸序列,这些可以通过量子化学计算、片段对接计算,以及从天然蛋白中提取来获得。
科学家重点关注第二步:运用给定的功能位点信息,设计折叠成包含该位点的三维(3D)结构的氨基酸序列。 从头设计功能性蛋白的难题是能够提出一个有稳定功能区域(活性位点、结合界面等)的整体骨架,并设计折叠成该结构的序列。但通常这这个过程分成两步。
因此,理想的功能性蛋白不仅能将功能位点嵌入蛋白质骨架中,以保持最小的形变,且蛋白质骨架具有多样性,还能同时生成骨架结构和氨基酸序列。
基于上述要求,研究人员使用两种深度学习方法来设计功能蛋白。
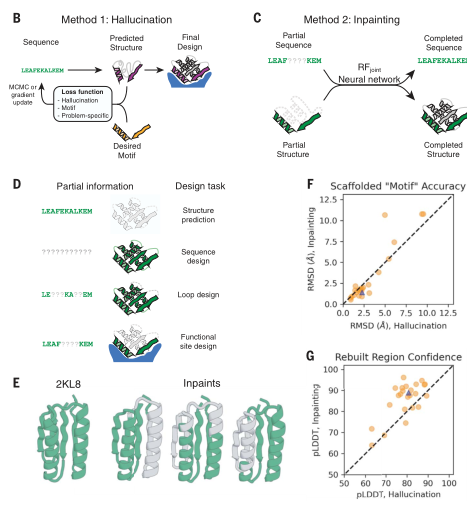
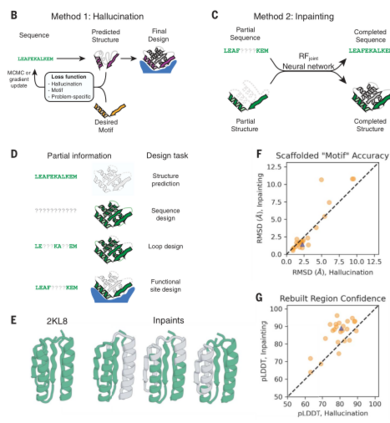
第一种方式是**“Hallucination”**(幻觉,预测优化):通过限制功能区域的片段结构,用复合损失函数优化氨基酸序列,以折叠到包含所需功能位点的结构,AI经过不断地迭代和优化,得到稳定的目标蛋白,并能在实验室中制造和研究。
简单来说,就像是对胡言乱语的单词强加一些要求,然后计算机通过不断地设计和改变,使之有意义,最终得到一个完整的故事。
第二种被称为**“ Inpainting”(修复,蛋白质修复):即将特定的序列/活性位点输入到软件(RoseTTAFold神经网络)中,软件可以在几秒内填补蛋白质结构的缺失部分,类似于使用语言模型补全给定的几个单词,该方法将蛋白质设计简化为信息缺失—恢复问题。**
Hallucination和Inpainting的流程图
两种方式没有高低优劣之分。
Hallucination(幻觉)耗费的算力更大,每次设计需要5—20分钟,但准确度更高。因此当信息缺失区域更大时,Hallucination的效果更好,产生的蛋白质结构也更具多样性。
02、应用案例及展望
实验测试表明,通过幻觉和修复产生的许多蛋白质都按预期发挥作用,包括生成潜在的潜在的RSV疫苗、金属结合蛋白、酶、以及结合PD-1 受体的蛋白质,这些设计的蛋白不仅能够表达特定功能,在结构和序列上和天然蛋白也有较大的差距。
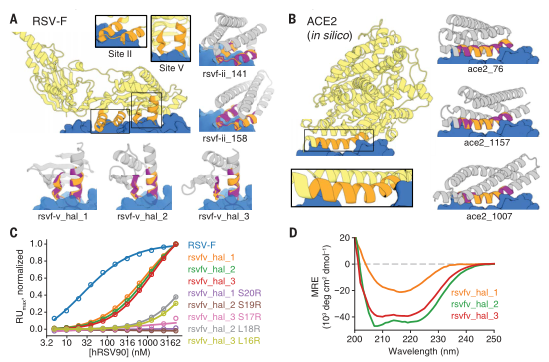
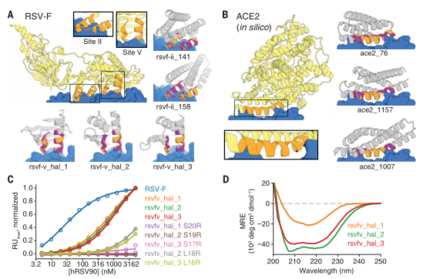
例如对呼吸道合胞病毒(RSV)的验证,研究人员针对其抗原表位用AI设计了37个新兴蛋白质,其中三个以0.9-1.3μM的结合力与RSV的中和抗体结合,为相关疫苗开发提供新的思路。
(淡黄色—天然蛋白质支架,橙色——天然功能基序,灰色—幻觉设计的支架,紫色—幻觉设计的功能基序)
“通过这两种方式,可以在新设计的蛋白质中得到关键特征,这些特征可以是已知的结合基序,甚至是酶活性位点。”研究人员解释。
可以说,本篇文章证明深度学习可用于设计具有多种功能的蛋白质,包括制造出可用作疫苗、癌症治疗甚至是消除空气中碳污染的工具的蛋白质,对药物研发和合成生物学都有重要的应用。
“这些都是非常强大的新方法,但仍有很大的改进空间,”论文通讯作者David Baker说道,“例如,设计高活性酶仍然非常具有挑战性。”
值得一提的是,这篇论文已经是今年Baker课题组在Science发布的第三篇文章,整个课题组已经从蛋白质结构预测逐渐转型为蛋白质设计。
本篇文章中也集成了课题组此前的工作,包括hallucination的蛋白质设计方法,从靶点结构设计蛋白质等。参考资料:DOI:10.1126/science.abn2100 https://www.technologynetworks.com/drug-discovery/news/scientists-train-ai-to-generate-medicines-and-vaccines-363979