样本收集策略
【1562】【必须收藏】IASLC:为肺癌个体化治疗执行PD-L1检测指南
编译:Jimmy
编译自:IASLC ATLAS of PD-L1 IHC in Lung Cancer
随着基于患者分子特征的个体化治疗的发展,过去十年晚期肺癌的治疗得到极大进展。现在很多患者可以接受更低毒性的治疗,得到更长疾病控制及生存获益,而且有些患者有望治愈。伴随着个体化治疗,随之而来的是日益增多且更为复杂的检测。因此,病理学家在日常肺癌诊断中的角色也发生明显变化。活检组织的最佳处理、组织切片的分层、生物标志物分析的优先顺序在病理工作流程及诊断中都尤为重要。
在临床实践中,非小细胞肺癌患者选择靶向治疗需要进行EGFR突变及ALK、ROS基因重排检测(Lindeman 2013)。EGFR检测的DNA可以从血浆或者肿瘤组织中分离,就组织而言,通常需要很多数量(10张或者更多)的未染色的组织切片或者细胞蜡块切片。当前的ALK和ROS1检测通常使用IHC或者FISH检测,只需要1至2张未染色切片(Tsao 2016)。根据指南建议,EGFR、ALK和ROS1异常检测仅仅用于腺癌或者腺癌成分不能排除(例如在活检样本中)的非小细胞肺癌,或者有EGFR突变、ALK或ROS1重排高风险的鳞癌患者(例如从不或者很少吸烟或者年轻女性尤其亚裔人群)。尽管曾有报道鳞癌中有EGFR和ALK基因异常,但基于发生率低和费用考虑,其不被推荐作为常规检测。既往鳞癌不做生物标志物检测的模式已经改变,鳞癌同样也需要进行PD-L1检测。
检测更多的新生物标志物对于小的活检样本影响最大,因为每个样本的组织成分数量有限,并且在重切蜡块时不可避免会损耗组织。(Kim 2014).
国际肺癌研究协会、美国胸部肿瘤协会、欧洲呼吸协会和WHO(Travis 2011; Travis 2015)共同合作,制定了如何保存活检组织标本以便用于预测生物标志物检测的明确指南。
尤为重要的是,病理科要制定策略使分子生物标志物检测融入到日常组织处理工作中,将肿瘤诊断和分类所需附属特殊染色数量最小化。通常,对于鉴别分化差的非小细胞肺癌为倾向鳞癌或者腺癌,使用2-4种染色(TTF-1、P40或者P63,有或者无mucin和CK5表达)已足够(Loo 2010; Rekhtman 2011)。通常根据H&E的初始结果,借助额外IHC染色(例如CD56、嗜金属鉻粒蛋白、突触素)来诊断和鉴别神经内分泌癌 (Travis 2011; Thunnissen 2017)。最终仅需要额外的2-4张白片用于普通肺癌的常规组织诊断,这样应该能够为包括PD-L1表达检测在内的生物标志物检测进一步提供大量额外切片。(图1)
图1. IHC检测对肺癌患者治疗时的诊断考虑不可或缺
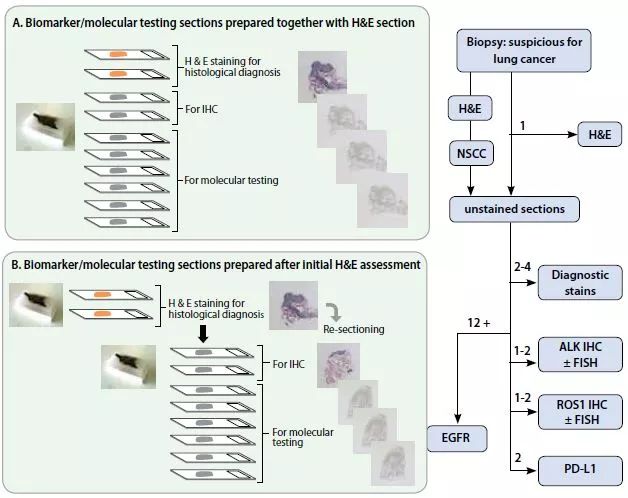
实验室可以在初始切片时准备10张或更多未染色切片(用于H&E染色以外的1张白片除外)以便用于生物标志物检测在内的辅助研究。另一种方法是病理医生初步诊断H&E 染色片之后,实验室为辅助诊断 及生物标志物检测进一步切片。(Figure 2)第一种方法可能给非肿瘤或无症状样本带来不必要的切片,并且要为所有额外样本保证足够的储存空间。第二种方法可能增加初期诊断和生物标志物检测结果的周转时间。生物标志物检测策略(无论是病理医生申请的反射性检测还是 肿瘤医生申请的检测)也和样本准备 流程息息相关。保存6周以上的白片可能不适用于大多数包括IHC、FISH或者 DNA 测序在内的分子检测。
图2. 分子检测最大化利用组织的策略 :准备为分子检测的IHC白片可能在初始的HE染色评估之前(A)或者之后(B)。准备白片数量取决于病理科的策略,为最佳的组织使用和对初始诊断和生物标志物检测结果的最短周转时间
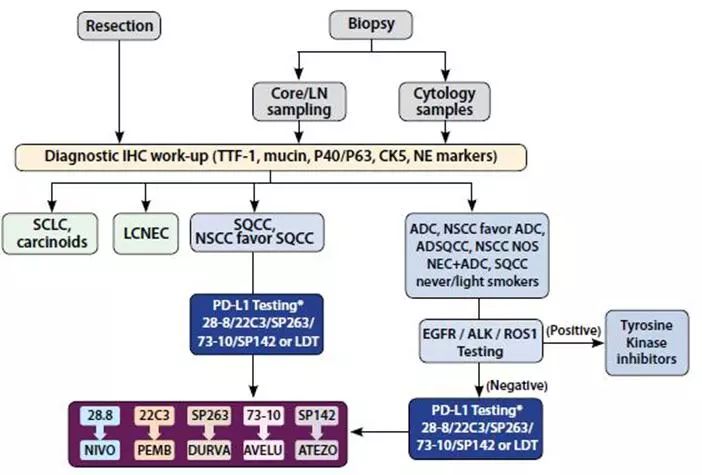
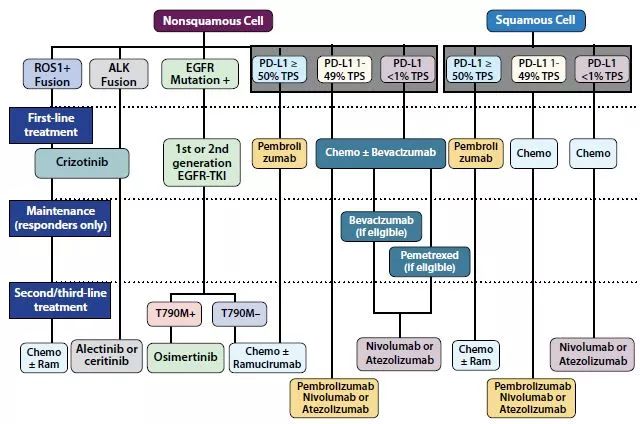
当前建议的任何治疗和生物标志物检测法则(图3)都可能由于该领域的迅速进展而快速过时。最近使PD-L1检测发挥重要作用的是帕姆单抗,获批用于PD-L1 TPS≥50%并且无EGFR突变和ALK重排的一线治疗。然而,在EGFR、ALK或者ROS1异常的患者中,决定PD-L1状态可能并不是必须的,除非已经用尽可选的靶向治疗,这类人群主要使用各自TKIs。病理医生可能希望在有这些异常的患者中推迟PD-L1检测,直到肿瘤科医生提出检测的需求。但是这种策略有潜在风险,因为当提出这项检测需求时,因为可能存放的白片已不适合进行PD-L1染色,或者组织蜡块由于EGFR检测而耗尽。
对于不存在EGFR、ALK或者ROS1异常的患者和既往已接受过一线或二线治疗的患者,只有帕姆单抗需要决定PD-L1表达(使用1%为域值)来限制治疗。但根据全球来看,PD-L1检测可能被肿瘤医生使用于纳武单抗治疗非鳞癌非小细胞肺癌的知情同意。一旦正在进行的5种抗PD-1/PD-L1药物的各项临床II期和III期试验得到结果,将来我们可能见证PD-L1检测法则更多的改变
图3 晚期NSCLC标准治疗法则(2017年1月提议)
结论
当前的PD-L1检测法则正在演变,并且一旦得到正在进行的临床试验结果可能发生巨大改变。然而病理实验室应该时刻准备更新关于组织管理和白片样本准备来适应PD-L1检测的策略,并且更新在日常临床实践中遇到的各种生物标志物的优先检测顺序策略。
Ming Sound Tsao, MD, FRCPC Keith M. Kerr, MB ChB, FRCPath, FRCPE Sanja Dacic, MD, PhD Yasushi Yatabe, MD, PhD Fred R. Hirsch, MD, PhD . ATSLC ATLAS of PD-L1 IHC in Lung Cancer. First IASLC Press Printing April 2017
Lindeman NI, Cagle PT, Beasley MB, et al. Molecular testing guideline for selection of lung cancer patients for EGFR and ALK tyrosine kinase inhibitors: guideline from the College of American Pathologists, International Association for the Study of Lung Cancer, and Association for Molecular Pathology. J Thorac Oncol. 2013;8(7): 823-859.
Tan DS, Yom SS, Tsao MS, et al. The International Association for the Study of Lung Cancer consensus statement
on optimizing management of EGFR mutation-positive non-small cell Lung cancer: Status in 2016. J Thorac Oncol. 2016;11(7):946-963.
Kim L, Tsao MS. Tumour tissue sampling for lung cancer management in the era of personalised therapy: what is
good enough for molecular testing? Eur Respir J. 2014; 44(4):1011-1022.
28个肿瘤相关临床试验招募患者
点击下方图片即可查看详情