研究发现Stat6乙酰化调控抗肿瘤免疫反应新机制
9月25日,国际学术期刊《自然-通讯》(Nature Communications)在线发表了中国科学院上海营养与健康研究所肖意传研究组与秦骏研究组合作的最新研究成果“Modulation of M2 macrophage polarization by the crosstalk between Stat6 and Trim24”。该研究揭示了Stat6乙酰化调节巨噬细胞M2极化,进而影响体内抗肿瘤免疫的作用机理,为抗肿瘤免疫的调控提供了新的分子靶标。
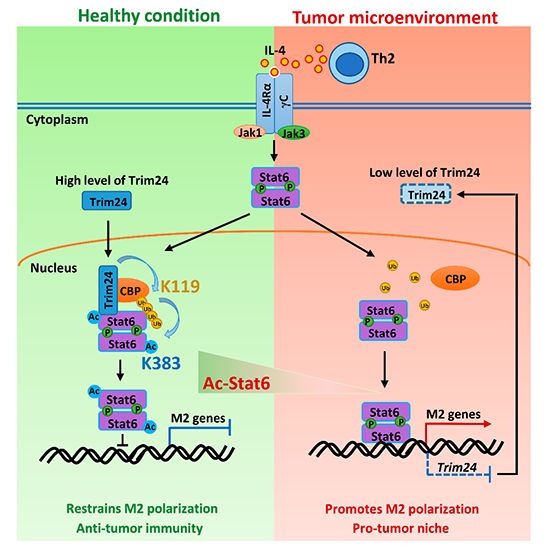
肿瘤微环境中的免疫细胞构成了肿瘤中的免疫调节系统,其中具有M2型特征的TAMs(tumor associated macrophages, TAMs)在抑制抗肿瘤免疫并促进肿瘤进程中起到了重要的调控作用,然而TAMs向M2极化精细调控的分子机制仍不清楚。该研究发现在巨噬细胞M2型极化过程中,调控极化的关键转录因子Stat6可以发生CBP介导的K383位点乙酰化修饰,该位点的乙酰化修饰能够明显抑制Stat6的转录活性以及下游M2型特征基因的表达。随后,通过高通量转录组测序(RNA-seq)结合蛋白质谱分析,研究人员发现了一种Trim家族蛋白的E3泛素连接酶Trim24能够与乙酰基转移酶CBP结合,介导CBP蛋白K119位点K63连接的泛素化修饰,增强CBP对Stat6的招募并促进CBP介导的Stat6蛋白K383位点乙酰化修饰,从而抑制Stat6的转录活性以及巨噬细胞的M2型极化。
进一步的体内研究表明,Trim24基因在巨噬细胞中缺失后抑制了肿瘤微环境TAMs中Stat6蛋白K383位点的乙酰化修饰,进而促进了TAMs向M2方向的极化,由此促进了肿瘤的生长。研究人员还发现,乳腺癌病人肿瘤组织中TAMs相较癌旁正常组织中巨噬细胞表达更低水平TRIM24与更高水平的M2基因,且肿瘤细胞条件性培养基能明显抑制人单核或巨噬细胞中TRIM24表达。这些结果提示肿瘤微环境可能通过抑制TAMs中Trim24的表达进而抑制Stat6的乙酰化,从而进一步促进了TAMs向M2方向极化,并维持了肿瘤中免疫抑制性的微环境状态。因此,靶向Stat6乙酰化修饰或者Trim24活性可以作为肿瘤免疫干预的潜在分子靶标。
营养与健康所博士后于涛和博士生甘叔诚、朱清晨为论文共同第一作者,研究员肖意传和秦骏为共同通讯作者。该研究得到江苏大学附属医院教授毛朝明、上海交通大学医学院附属瑞金医院教授沈坤炜等的大力帮助。该研究还得到科技部、国家自然科学基金委及中科院等的资助,同时也得到营养与健康所公共技术平台和动物平台的支持。
Stat6乙酰化调节抗肿瘤免疫的分子机制
来源:中国科学院上海营养与健康研究所
温馨提示:近期,微信公众号信息流改版。每个用户可以设置 常读订阅号,这些订阅号将以大卡片的形式展示。因此,如果不想错过“中科院之声”的文章,你一定要进行以下操作:进入“中科院之声”公众号 → 点击右上角的 ··· 菜单 → 选择「设为星标」